下列图像表达正确的是( )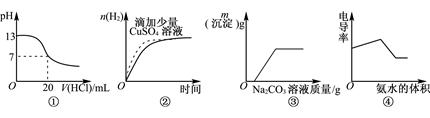
| A.图①表示25℃时,和0.1mol·L-1盐酸滴定20mL 0.1mol·L-1NaOH溶液 |
| B.图②表示常温下,等量锌粉与足量的等体积等浓度的盐酸反应 |
| C.图③表示向CaCl2和盐酸的混合溶液中滴加Na2CO3溶液 |
| D.图④表示向盐酸和醋酸混合溶液中滴入氨水 |
下列说法错误的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH小于4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.200 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度: ④>①>②>③ |
等体积,浓度均为0.1mol/L的三种溶液:
①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液,已知将①、②分别与③混合,实验测得产生的CO2气体体积[(v)随时间(t)变化的示意图所示,
下列说法正确的是
| A.物质酸性的比较:CH3COOH>HSCN>H2CO3 |
| B.反应结束后所得两溶液中,c(CH3COO—)>c(SCN—) |
| C.上述三种溶液中由水电离的c(OH—)大小:NaHCO3>CH3COOH>HSCN |
| D.CH3COOH溶液和NaHCO3溶液反应所得溶液中: |
c(CH3COO—)+c(CH3COOH)=0.10mol·L-1
下列说法正确的是
| A.物质的量浓度均为0.1mol·L-1的(NH4)2SO4、(NH4)2Fe(SO4)2两种溶液中,c(NH4+)相同 |
| B.25℃时,在0.1mol·L-1的CH3COOH溶液中加入CH3COONa固体,溶液的pH一定小与7 |
| C.25℃时,将0.1mol·L-1的NaOH溶液与pH=1的稀硫酸等体积混合,混合后的溶液pH=7 |
| D.将同浓度的NaAlO2溶液与Na2CO3溶液混合后,可以生成白色沉淀,并产生气泡 |
一定温度下,向质量分数为a的乙腈(CH3CN)溶液中加入等体积水,所得溶液中乙腈质量分数为0.4a,则乙腈的密度(ρ1)与水的密度(ρ2)的关系是
| A.ρ1>ρ2 | B.ρ1=ρ2 | C.ρ1<ρ2 | D.无法确定 |
常温下,对下列四种溶液的叙述正确的是 ( )
| |
① |
② |
③ |
④ |
| 溶液 |
氨水 |
氢氧化钠溶液 |
醋酸溶液 |
盐酸 |
| pH |
11 |
11 |
3 |
3 |
A.②、③两溶液相比,溶液中水的电离程度不相同
B.四种溶液分别加水稀释10倍,pH变化最大的是①和⑧
C.①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D.①、④两溶液按一定体积比混合,所得溶液中离子浓度的关系不存在:
c(H+)>c(Cl—)>c(OH—)>c(NH+4)
下列关于电解质溶液说法正确的是 ( )
| A.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
| B.等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB |
| C.常温下,弱酸酸式盐NaHA溶液的pH=6,说明HA‾的电离程度大于其水解程度 |
| D.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水的电离程度相同 |
常温下,将氨水滴加到盛有AgCl浊液的试管中,AgCl逐渐溶解,再加入NaBr溶液又产生了浅黄色沉淀。下列说法不正确的是
| A.AgCl的溶解度大于AgBr的溶解度 |
| B.若在AgBr浊液中,加入氨水浅黄色沉淀溶解 |
| C.AgCl和AgBr见光都易分解 |
| D.AgCl与氨水反应生成Ag(NH3)2+,故氨水能使AgCl溶解 |
根据以下事实得出的判断一定正确的是 ( )
A.0.1mol/LNaHCO3溶液中,c(OH-)-C(H+)=c(H2CO3)-c(CO32-) |
B.A+和B-的电子层结构相同,则A原子的核电荷数比B原子的小 |
C.A盐的溶解度在同温下比B盐的大,则A盐溶液的物质的量浓度比B盐溶液的大 |
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强 |
25℃时,用0.2mol/L HC1溶液滴定25mL 0.1mol/LNaOH溶液,右图是溶液的pH与加入HC1溶液的体积关系,图中Ⅰ、Ⅱ、Ⅲ分别代表实验不同阶段的溶液。下列有关说法不正确的是( )
| A.图中Ⅰ点对应的纵坐标a=13 |
| B.图中Ⅱ点对应的横坐标b=12.5 |
| C.图中Ⅲ点所示溶液中:c(C1—)=2e(Na+) |
| D.图中Ⅱ、Ⅲ间的任意一点所示溶液中: |
c(Na+)>c(C1—)>c(H+)>c(OH—)
今有室温下四种溶液,有关叙述不正确的是
| |
① |
② |
③ |
④ |
| 浓度c/mol/L |
0.1 |
0.1 |
0.1 |
0.1 |
| 溶液 |
氨水 |
CH3COONa溶液 |
醋酸 |
盐酸 |
| A.在20mL①溶液中逐滴加入③溶液,溶液导电能力变化如下图(1)所示 |
| B.②、③两溶液等体积混合,离子浓度:2c(Na+)=c(CH3COO-)+c(CH3COOH) |
C.用③滴定①,用酚酞作指示剂,滴定曲线如下图(2)所示: |
| D.①、④两溶液等体积混合,离子浓度:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后,下列关系式中正确的是
| A.c(Na+)=c(CH3COO-)+c(CH3COOH) | B.c(H+)=c(CH3COO-)+c(OH-) |
| C.c(Na+)>(CH3COO-)>c(OH-)>c(H+) | D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
下列叙述正确的是
| A.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合: 2c(Na+) + c(CH3COOH) = c(CH3COO-) +2c(OH-) |
| B.Ksp(AgCl)>Ksp(AgI)由此可以判断AgCl(S) + I- = AgI(S) + Cl-能够发生 |
| C.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| D.中和浓度与体积均相等的盐酸和醋酸溶液,消耗NaOH的物质的量不相等 |
试题篮
()