2008年1月8日,国家主席胡锦涛在人民大会堂为获得2007年国家最高科学技术奖的石油化工催化剂专家闵恩泽教授颁奖,以表彰他在催化剂研究方面做出的突出贡献。下列关于催化剂的说法正确的是
| A.使用催化剂可以增大正反应速率,减小逆反应速率 |
| B.使用催化剂可以使化学平衡正向移动 |
| C.使用催化剂可以降低反应的活化能 |
| D.使用催化剂可以改变反应的平衡常数 |
下列关于平衡常数的说法正确的是
| A.改变外界条件使化学平衡状态改变时,平衡常数也一定改变 |
| B.改变条件,反应物的转化率增大,平衡常数一定增大 |
| C.若一个可逆反应的平衡常数很大,则反应会在较短的时间内完成 |
D.已知2NO2 N2O4正反应的平衡常数为K1,逆反应的平衡常数为K2,则K1=1/K2 N2O4正反应的平衡常数为K1,逆反应的平衡常数为K2,则K1=1/K2 |
在一定温度下的恒容容器中,表明反应A(s)+2B(g)  C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
| A.混合气体的压强不随时间变化而变化 |
| B.混合气体的密度不随时间变化而变化 |
| C.气体总物质的量不随时间变化而变化 |
| D.单位时间内生成n mol C,同时消耗2n molB |
可逆反应3H2+N2 2NH3达到平衡的标志是
2NH3达到平衡的标志是
①消耗3 mol H2的同时生成2 mol NH3
②1个N≡N键断裂的同时,有3个H-H键形成
③H2、N2与NH3的物质的量之比为3∶1∶2
④1个N≡N键断裂的同时,有6个N-H键断裂
⑤1个N≡N键断裂的同时,有6个N-H键形成
| A.①②⑤ | B.②④ | C.①②③④ | D.全部 |
对于反应COCl2(g) CO(g)+Cl2(g)。改变下列条件:①升温 ②恒容下通入惰性气体③增加COCl2浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体,能加快反应速率的是
CO(g)+Cl2(g)。改变下列条件:①升温 ②恒容下通入惰性气体③增加COCl2浓度 ④减压 ⑤加催化剂 ⑥恒压下通入惰性气体,能加快反应速率的是
| A.①②⑤ | B.①③⑤ | C.②④⑥ | D.③⑤⑥ |
一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
2NH3(g) ΔH<0,反应过程如图,下列说法正确的是
| A.t1 min时正、逆反应速率相等 |
| B.X曲线表示NH3的物质的量随时间变化的关系 |
| C.0~8 min,H2的平均反应速率v(H2)=0.01mol·L-1·min-1 |
| D.10~12 min,升高温度使反应速率加快,平衡正向移动 |
在恒容密闭容器中发生反应2SO2+O2  2SO3,当其他条件不变时,只改变一个条件,不能加快化学反应速率的是
2SO3,当其他条件不变时,只改变一个条件,不能加快化学反应速率的是
| A.增加SO2的浓度 | B.充入一定量惰性气体 |
| C.升高温度 | D.使用催化剂 |
在容积固定的密闭容器中发生反应:2NO+O2 2NO2,不能判断该反应达到到平衡状态的是
2NO2,不能判断该反应达到到平衡状态的是
| A.单位时间内生成n molO2的同时,生成2n mol NO2 |
| B.NO2、NO、O2反应速率的比为2∶2∶1 |
| C.混合气体的颜色不再改变的状态 |
| D.混合气体的压强不再改变的状态 |
在一体积可变的密闭容器中,通入1molN2和3molH2,发生反应N2+3H2 2NH3,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率与时间的关系曲线正确的是
2NH3,在t1时刻达到平衡。保持温度和压强不变,在t2时刻,再通入一部分NH3,反应速率与时间的关系曲线正确的是
将BaO2放入密闭的真空容器中,反应2BaO2(s) 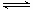 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
| A.BaO2量增加 | B.BaO量不变 | C.氧气压强不变 | D.平衡常数减小 |
在恒容密闭容器中,反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0达到平衡后,改变某一条件,下列说法正确的是
CH3OH(g)+H2O(g) △H<0达到平衡后,改变某一条件,下列说法正确的是
| A.升高温度,正反应速率减小,逆反应速率增加,平衡逆向移动 |
| B.升高温度,可提高CO2转化率 |
| C.增加H2的浓度,可提高CO2转化率 |
| D.改用高效催化剂,可增大反应的平衡常数 |
一定条件下,某反应达到化学平衡时,下列说法错误的是
| A.反应停止了 | B.各物质的浓度不再改变 |
| C.正反应速率等于逆反应速率 | D.该反应达到最大限度 |
下列选择的条件符合勒夏特列原理的是
| A.硫酸工业中合成三氧化硫采用常压条件 |
| B.合成氨工业采用高压 |
| C.硫酸工业选用浓硫酸吸收三氧化硫 |
| D.合成氨工业采用500度左右的温度 |
试题篮
()