可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是:
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是: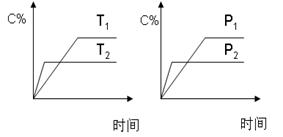
| A.达到平衡后,加入催化剂则C%增大 |
| B.达到平衡后,若升高温度,平衡向右移动 |
| C.化学方程式中b < c +d |
| D.达平衡后,增加A的量,有利于平衡向右移动 |
I2在KI溶液中存在平衡:I2(aq)+I-(aq) I3- (aq),某I2、、KI混合溶液中, c(I3-)与温度T的平衡曲线图如下。下列说法不正确的是
I3- (aq),某I2、、KI混合溶液中, c(I3-)与温度T的平衡曲线图如下。下列说法不正确的是
A.反应I2(aq)+I-(aq) I3- (aq)的△H>0 I3- (aq)的△H>0 |
B.若温度为 ,反应的平衡常数分别为 ,反应的平衡常数分别为 |
C.若反应进行到状态D时,一定有 |
| D.状态A与状态B相比,状态A的c(I2) 小 |
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)⇌SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示.由图可得出的正确结论是( )
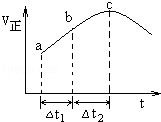
| A.反应在C点达到平衡状态 |
| B.反应物浓度:a点小于B点 |
| C.反应物的总能量低于生成物的总能量 |
| D.△t1=△t2时,SO2的转化率:a~B段小于B~C段 |
某密闭容器中发生如下反应:2X(g)+Y(g)  Z(g);△H <0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是
Z(g);△H <0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是 
| A.t3时减小了压强 |
| B.t5时增大了压强 |
| C.t6时刻后反应物的转化率最低 |
| D.t1 - t2时该反应的平衡常数大于 t6 时反应的平衡常数 |
下列图示与对应的叙述一定正确的是()
A.图1所示,反应X(g)+2Y(g) 3Z(g),b的压强一定比a大 3Z(g),b的压强一定比a大 |
| B.图2表示CO生成CO2的反应过程和能量关系 |
C.图3表示反应CO+2H2 CH3OH,其中温度T1>T2,在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,平衡正向移动,氢气浓度增大 CH3OH,其中温度T1>T2,在其他条件不变的情况下,将处于E点的体系的体积压缩到原来的1/2,平衡正向移动,氢气浓度增大 |
| D.图4所示,用水稀释pH相同的盐酸和醋酸,I表示盐酸,II表示醋酸,且溶液导电性c>b>a |
某温度下,H2(g)+CO2(g)  H2O(g)+CO(g)的平衡常数K=9/4.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.
H2O(g)+CO(g)的平衡常数K=9/4.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如下表所示.
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)(mol/L) |
0.010 |
0.020 |
0.020 |
| c(CO2)(mol/L) |
0.010 |
0.010 |
0.020 |
下列判断不正确的是( )
A.平衡时,乙中CO2的转化率大于60%
B.平衡时,甲中和丙中CO2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
在温度相同,压强分别为P1和P2的条件下,A(g)+2B(g) nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是( )
nC(g)的反应体系中,C的百分含量(c%)与时间t的曲线如右图所示,下面结论正确的是( )
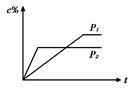
| A.P1>P2,n<3 | B.P1<P2,n>3 |
| C.P1>P2,n>3 | D.P1<P2,n<3 |
温度和压强对X + Y 2Z反应的影响,如图所示。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列对于该反应的叙述正确的是
2Z反应的影响,如图所示。图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列对于该反应的叙述正确的是
| A.正反应为放热反应 | B.X、Y、Z均为气体 |
| C.X和Y中只有一种是气态,Z为气态 | D.逆反应的ΔH > 0 |
根据下列有关图象,说法正确的是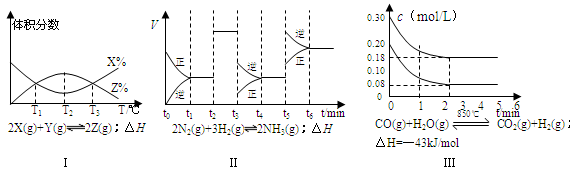
| A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0 |
| B.由图Ⅱ知,反应在t6时,NH3体积分数最大 |
| C.由图Ⅱ知,t3时采取降低反应温度的措施 |
| D.图Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出51.6kJ的热量 |
一定温度下,把2. 0体积的N2和6. 0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2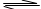 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是
| A.1.0体积的N2和3.0体积的H2 | B.2.0体积的N2、6.0体积的H2和4.0体积的NH3 |
| C.4.0体积的NH3和1.0体积的H2 | D.2.0体积的NH3 |
如图表示反应M(g)+P(g) nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是
nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是
A.通过分析上图,该反应的正反应为放热反应
B.A状态与C状态的化学反应速率比较为v(A)<v(C)
C.在T 1、D状态时,v正<v逆
D.在T2、B状态时,改变体积始终有v正=v逆,则n=2
在一密闭容器中加入A、B、C三种气体,在温度为T K和(T+10)K时,测得各物质的浓度如下表,据此得出的下列结论中正确的是
| 温度 |
T K |
(T+10)K |
|||
| 测定时刻/s |
t1 |
t2 |
t3 |
t4 |
t5 |
| c(A)/mol·L-1 |
6 |
3 |
2 |
2 |
2.2 |
| c(B)/mol·L-1 |
5 |
3.5 |
3 |
3 |
3.1 |
| c(C)/mol·L-1 |
1 |
2.5 |
3 |
3 |
2.9 |
A.在t3时刻反应已经停止
B.升高温度,该反应的化学平衡常数将增大
C.在t 3时刻,若增大压强,则A的转化率将减小
D.在t2~ t3内,A的平均反应速率为 mol·(L·s)-1
mol·(L·s)-1
已知某可逆反应mA(g)+ nB(g)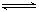 pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )
pC(g),在密闭容器中进行,下图表示在不同反应时间t、温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线,由曲线分析,下列判断正确的是( )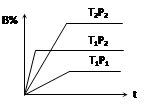
| A.T1<T2、P1>P2、m+n>p,⊿H <0; |
| B.T1>T2、P1<P2、m+n>p,⊿H >0; |
| C.T1>T2、P1<P2、m+n<p,⊿H >0; |
| D.T1<T2、P1>P2、m+n<p,⊿H <0; |
相同温度下,容积均恒为2L的甲、乙、丙3个密闭容器中发生反应:2SO2(g)+O2(g) 2SO3(g)△H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
2SO3(g)△H=-197kJ·mol-l。实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
| A.Q1>Q3>Q2 =78.8kJ |
| B.三个容器中反应的平衡常数均为K=2 |
| C.甲中反应达到平衡时,若升高温度,则SO2的转化率将大于50% |
| D.若乙容器中的反应经tmin达到平衡,则0~tmin内,v(O2)=1/(5t) mol/(L·min) |
反应N2O4(g) 2NO2(g)⊿H = +57KJ/mol,在温度为
2NO2(g)⊿H = +57KJ/mol,在温度为 、
、 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是 ( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C
试题篮
()