一定温度下,在一个体积可变的密闭容器中加入2 mol N2和2 mol H2,建立如下平衡:N2(g)+3H2(g) 2NH3(g)相同条件下,若向容器中再通入1 mol N2和1 mol H2,又达到平衡。则下列说法正确的是
2NH3(g)相同条件下,若向容器中再通入1 mol N2和1 mol H2,又达到平衡。则下列说法正确的是
| A.NH3的百分含量不变 | B.N2的体积分数增大 |
| C.H2的转化率增大 | D.NH3的百分含量增大 |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2 + O2 2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法不正确的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法不正确的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.化工生产中,可通过改变温度、浓度、压强等因素,提高SO2的转化率 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
下列有关叙述正确的是( )
A.在一定条件下,反应CO(g)+2H2(g)  CH3OH(g)在一密闭容器中达到平衡,充入适量氢气,增大容器的体积,维持H2的浓度和容器的温度不变,原平衡相比较达新平衡时CO的转化率不变 CH3OH(g)在一密闭容器中达到平衡,充入适量氢气,增大容器的体积,维持H2的浓度和容器的温度不变,原平衡相比较达新平衡时CO的转化率不变 |
| B.常温下:pH=12的NaOH溶液和pH=2的醋酸混合后恰好完全反应(不考虑溶液体积的变化),反应后的溶液中:c(CH3COO-)+ c(CH3COOH)=0.01mol/L |
| C.pH相同的①CH3COONa;②NaHCO3;③NaAlO2三份溶液中的c(Na+):③>②>① |
| D.已知某温度下:Ksp(AgCl)=1.56×10-10, Ksp(Ag2CrO4)= 1×10-12,,将0.001mol/L的AgNO3溶液逐滴滴入0.001mol/L的KCl和0.001mol/LK2CrO4溶液,则先产生Ag2CrO4沉淀 |
在某容积可变的密闭容器中,有下列的可逆反应:A(g) + B(g)  xC(g),有图1(T表示温度,P表示压强,C%表示C的体积分数)所示的反应曲线。若试判断对图2的说法中正确的是
xC(g),有图1(T表示温度,P表示压强,C%表示C的体积分数)所示的反应曲线。若试判断对图2的说法中正确的是 
| A.P3>P4,y轴表示C的体积分数 |
| B.P3<P4,y轴表示B的质量分数 |
| C.P3<P4,y轴表示混合气体的密度 |
| D.P3>P4,y轴表示混合气体的平均摩尔质量 |
一定温度下的恒容密闭容器中,可逆反应2NO2(g) 2NO(g)+ O2(g)达到平衡状态的标志是
2NO(g)+ O2(g)达到平衡状态的标志是
①2V(O2)=V(NO2)
②单位时间内生成n molO2的同时生成2n molNO2
③NO2、NO、O2的浓度之比为2∶2∶1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变
| A.②④⑥ | B.①④⑥ | C.②④⑤ | D.全部 |
还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下:
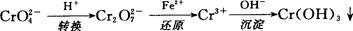
已知转化过程中的反应为
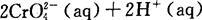
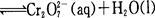 [MCr=52,M(FeS04·7H2O)=278]
[MCr=52,M(FeS04·7H2O)=278]
转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是
| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeS04·7H2O)作还原剂,处理1 L废水,至少需要458.7g |
| C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=6 |
| D.2V正(CrO42-)= V逆(Cr2O72-)时,反应处于平衡态 |
可逆反应mA(g)十nB(g) pC(g)十qD(g)的v-t图象如下右图,若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图。对于下列命题:
pC(g)十qD(g)的v-t图象如下右图,若其它条件不变,只是在反应前加入合适的催化剂,则其v-t图象如图。对于下列命题:
①a1>a2 ②a1<a2 ③b1>b2 ④b1<b2 ⑤t1>t2 ⑥t1﹦t2 ⑦两图中阴影部分面积相等 ⑧右图中阴影部分面积更大。以上说法中正确的是

| A.②④⑤⑦ | B.①④⑥⑧ | C.②③⑤⑧ | D.①③⑥⑦ |
硫酸生产中,其尾气是大气污染来源之一,2SO2(g)+O2(g) 2SO3(g)。现在一种新型纳米材料氧缺位铁酸盐CoFe2OX由铁酸盐CoFe2O4经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。下图是某温度下SO2的平衡转化率(a)与体系总压强(p)的关系,下列说法正确的是
2SO3(g)。现在一种新型纳米材料氧缺位铁酸盐CoFe2OX由铁酸盐CoFe2O4经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去。下图是某温度下SO2的平衡转化率(a)与体系总压强(p)的关系,下列说法正确的是
A.新型纳米材料氧缺位铁酸盐CoFe2OX的X的值是5
B.新型纳米材料氧缺位铁酸盐CoFe2OX在将酸性氧化物分解除去的过程中起催化作用
C.温度升高,SO2浓度增大,该反应的焓变为正值
D.平衡状态由A变到B时,平衡常数K(A)=K(B)
在100℃时,将N2O4、NO2分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g)  N2O4(g) ΔH <0]
N2O4(g) ΔH <0]
| 容器 |
物质 |
起始浓度/(mol·L-1) |
平衡浓度/(mol·L-1) |
| Ⅰ |
N2O4 |
0.100 |
0.040[ |
| NO2 |
0 |
0.120 |
|
| Ⅱ |
N2O4 |
0 |
0.014 |
| NO2 |
0.100 |
0.072 |
下列说法正确的是
A.平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2)
B.平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数K(Ⅰ) = 2K(Ⅱ)
C.平衡后,升高相同温度,以N2O4表示的反应速率ν(Ⅰ)<ν(Ⅱ)
D.平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
有一反应:2A+B 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是 
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下若由a点达到平衡,可以采取增大压强的方法
D.c点v (正)<v (逆)
在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率v(B)= 0.04 mol·L-1·min-1
B.图Ⅱ所知反应xA(g)+yB(g) zC(g)的△H<0,且a=2
zC(g)的△H<0,且a=2
C.若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆)
D.200℃时,向容器中充入2 mol A 和1 mol B,达到平衡时,A 的体积分数小于0.5
已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量的NO2气体,且起始时体积相同。发生反应:2NO2(g) N2O4 (g) △H<0。一段时间后相继达到平衡状态。下列说法中正确的是
N2O4 (g) △H<0。一段时间后相继达到平衡状态。下列说法中正确的是
| A.平衡时NO2体积分数:甲<乙 |
| B.达到平衡所需时间,甲与乙相等 |
| C.该反应的平衡常数表达式K=c(N2O4)/c(NO2) |
| D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态 |
ToC时,在一固定容积的密闭容器中发生反应:A(g)+B(g) X(s) ∆H < 0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,则判断正确的是
X(s) ∆H < 0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,则判断正确的是
A.ToC时,该反应的平衡常数值为4
B.c点没有达到平衡,此时反应向逆向进行
C.若c点为平衡点,则此时容器内的温度高于ToC
D.ToC时,在d点加入一定量X可达到c点
相同容积的四个密闭容器中进行同样的可逆反应:2X(g)+Y(g) 3W(g)+2Z(g)起始时四个容器所装X、Y的量分别为:甲(X:2mol,Y:1mol) 乙(X:1mol,Y:1mol)丙(X:2mol,Y:2mol) 丁(X:1mol,Y:2mol)在相同温度下,建立平衡时,X或Y的转化率大小关系为
3W(g)+2Z(g)起始时四个容器所装X、Y的量分别为:甲(X:2mol,Y:1mol) 乙(X:1mol,Y:1mol)丙(X:2mol,Y:2mol) 丁(X:1mol,Y:2mol)在相同温度下,建立平衡时,X或Y的转化率大小关系为
| A.X的转化率为:甲<丙<乙<丁 | B.X的转化率为:甲<乙<丙<丁 |
| C.Y的转化率为:甲>丙>乙>丁 | D.Y的转化率为:丁>乙>丙>甲 |
试题篮
()