aX(g)+bY(g) cZ(g)+dW(g)在一定体积的密闭容器中反应5 min达到平衡时,X减少n mol·L-1,Y减少
cZ(g)+dW(g)在一定体积的密闭容器中反应5 min达到平衡时,X减少n mol·L-1,Y减少 mol·L-1,Z增加
mol·L-1,Z增加 mol·L-1。若将体系压强增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为
mol·L-1。若将体系压强增大,W的百分含量不发生变化。则化学方程式中各物质的化学计量数之比a∶b∶c∶d应为
| A.3∶1∶2∶1 | B.1∶3∶2∶2 |
| C.3∶1∶2∶2 | D.1∶3∶1∶2 |
在恒容密闭容器中,某反应在不同反应时间各物质的量浓度的变化情况如图所示(各物质均为气体)。请回答下列问题:
(1)该反应的化学方程式为 。
(2)反应开始至2分钟时,用C表示反应速率为 mol/(L•min),平衡时A的转化率为 。
(3)其它条件不变,当第3min条件发生以下变化时,能加快化学反应速率的是____。
①加入(正)催化剂 ②充入一定量He
③充入一定量的A ④降低温度
在一个0.5L密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和5.4 mol·L-1,在一定的条件下发生反应N2(g) + 3H2(g)  2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
2NH3(g)。10min后测得N2的浓度是0.8 mol·L-1,则在这10min内NH3的平均反应速率是
| A.0.1mol·L-1·min-1 | B.0.6mol·L-1·min-1 |
| C.0.3mol·L-1·min-1 | D.0.2mol·L-1·min-1 |
将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应2A(g)+B(g) 2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
2C(g),若2 s(秒)后测得C的浓度为0.6 mol/L,现有下列几种说法:
①用物质A表示反应的平均速率为0.3 mol/(L·s)
②用物质B表示反应的平均速率为0.6 mol/(L·s)
③2 s时物质A的转化率为70%
④2 s时物质B的浓度为0.7 mol/L
其中正确的是
| A.①③ | B.①④ | C.②③ | D.③④ |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是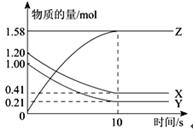
| A.反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s) |
| B.反应开始到10 s,X的物质的量浓度减少了0.79 mol/L |
| C.反应开始到10 s时,Y的转化率为79.0 % |
D.反应的化学方程式为:X(g)+Y(g) Z(g) Z(g) |
反应C(s)+H2O(g)  CO(g)+H2(g),在10L密闭容器中进行5分钟后,水蒸气的物质的量减少了0.45mol,则此反应的平均反应速率v(X)可表示为
CO(g)+H2(g),在10L密闭容器中进行5分钟后,水蒸气的物质的量减少了0.45mol,则此反应的平均反应速率v(X)可表示为
A.v(H2)=0.009mol• (L•s) -1 B.v(CO)=0.009mol• (L•min)-1
C.v(C)="0.00015" mol• (L•s) -1 D.v(H2O)=0.09mol• (L•min)-1
甲、乙两个容器内都在进行A→B的反应,甲中每分钟减少4 mol A,乙中每分钟减少2 mol A,则两容器中的反应速率
| A.甲快 | B.乙快 | C.相等 | D.无法确定 |
在体积为1 L的密闭容器中(体积不变)充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
| A.进行到3分钟时,正反应速率和逆反应速率相等 |
| B.10分钟后容器中各物质浓度不再改变 |
| C.达到平衡后,升高温度,正反应速率增大、逆反应速率减小 |
| D.3min前v正>v逆,3min后v正<v逆 |
对于A2+3B2 2C的反应来说,以下化学反应速率的表示中,反应速度最快的是
2C的反应来说,以下化学反应速率的表示中,反应速度最快的是
A.v(B2)="0.8" mol/(L·s) B.v(B2)= 3mol/(L·min)
C.v(C)="0.6" mol/(L·s) D.v(A2)="0.4" mol/(L·s)
下列措施对增大反应速率明显有效的是
| A.在K2SO4与BaCl2两溶液反应时,增大压强 |
| B.Fe与稀硫酸反应制取H2时,改用浓硫酸 |
| C.Al在氧气中燃烧生成A12O3,将Al片改成Al粉 |
| D.Na与水反应时增大水的用量 |
可逆反应2A(g)+3B(g)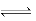 2C(g)+D(g)在四种不同条件下的反应速率分别为:
2C(g)+D(g)在四种不同条件下的反应速率分别为:
①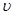 (A)="0.5" mol·L-l·min-l ②
(A)="0.5" mol·L-l·min-l ②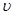 (B)="0.6" mol·L-l·min-l
(B)="0.6" mol·L-l·min-l
③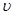 (C)="0.35" mol·L-l·min-l ④
(C)="0.35" mol·L-l·min-l ④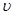 (D)="0.4" mol·L-l·min-l
(D)="0.4" mol·L-l·min-l
则该反应在不同条件下反应速率最快的是
A.① B.② C.③ D.④
反应A+3B=2C+2D在不同条件下反应速率如下,其中最快的是
| A.VA=0.15mol/(L·min) | B.VB=0.6mol/(L·min) |
| C.VC=0.4mol/(L·min) | D.VD="0.0075" mol/(L·s) |
在t℃时,10L 0.4mol·L-1H2O2溶液发生催化分解:2H2O2 = 2H2O + O2↑,不同时刻测得生成O2的体积如下表,已知反应至6min时,H2O2分解了50%(已折算为标准状况)
| t /min |
0 |
2 |
4 |
6 |
| V(O2)/L |
0.0 |
9.9 |
17.2 |
V=? |
下列叙述正确的是(溶液体积变化忽略不计)
A.0~2min H2O2平均反应速率比4~6min慢
B.反应至6min时,共产生O2 44.8L
C.0~6min的平均反应速率 v(H2O2)≈3.3×10-2mol·L-1·min-1
D.反应至6min时,c(H2O2) = 0.3mol·L-1
将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生反应:2A(g)+B(g)  2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:
2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3 mol/(L·s)
②用物质B表示的反应的平均速率为0.6mol/(L·s)
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol/L。其中正确的是
| A.①③ | B.②③ | C.①④ | D.②④ |
试题篮
()