A与B在容积为1 L的密闭容器中发生反应:aA(s)+bB(g)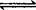 cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表: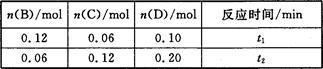
下列说法正确的是
A.0~t1时间段内,平均反应速率v(B)=O.04/t1 mol·(L·min)-1
B.若起始时n(D)=0,则t2时v(D)=0.20/t2 mol·(L·min)-1
C.升高温度,v(B)、vC)、v(D)均增大
D.b:d=6:1
在m A + n B  p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
p C的反应中,m、n、p为各物质的计量数。现测得C每分钟增加a mol/L,B每分钟减少1.5a mol/L,A每分钟减少0.5a mol/L,则m:n:p为
| A.2:3:2 | B.2:3:3 | C.1:3:2 | D.3:1:2 |
已知某反应的各物质浓度数据如下:aA(气)+ bB(气) = cC(气)
起始浓度(mol/L) 3.2 0.8 0.0
2s末浓度(mol/L) 2.0 0.4 0.8
由此可推算出上述方程式中各物质前面的化学计量数之比是
| A.1∶2∶4 | B.4∶1∶2 | C.3∶1∶2 | D.3∶2∶1 |
在恒温恒容的容器中进行反应H2 2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
2H,若反应物浓度由0.1mol/L降到0.06mol/L需20s,那么由0.06mol/L降到0.024mol/L,需反应的时间为
| A.等于18s | B.等于12s | C.大于18s | D.小于18s |
已知反应:PC15(g)  PC13 (g)+ C12(g),将1.0 mol PC15充入容积为2 L的密闭容器中,一段时间后,测得PC15的浓度为0.3 mol/L,在这段时间内的平均反应速率υ(PC15)=0.4 mol/(L·min),则这段时间为
PC13 (g)+ C12(g),将1.0 mol PC15充入容积为2 L的密闭容器中,一段时间后,测得PC15的浓度为0.3 mol/L,在这段时间内的平均反应速率υ(PC15)=0.4 mol/(L·min),则这段时间为
| A.50 s | B.30 s | C.5 s | D.1 s |
对于可逆反应A(g)+3B(g) 2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
A.v(A)=0.5 mol·L-1·min-1
B.v(C)=1.6mol·L-1·min-1
C.v(D)=0.4 mol·L-1·min-1
D.v(B)=1.8mol·L-1·min-1
在一定条件下,将A2和B2两种气体通入1 L密闭容器中,反应按下式进行:xA2+ yB2 ==2C(g), 两秒种后反应速率如下V(A2)=0.4mol/(L·s) V(B2)="=1.2" mol/(L·s) V(C)= 0.8mol/(L·s) 则该x和y的值分别为
A.2和3 B.3和2 C.3和1 D.1和3
一定条件下进行反应:A(g) B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
B(g)+C (g),向2.0 L恒容密闭容器中充入1.0 mol A(g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
| t/s |
0 |
2 |
4 |
6 |
8 |
| n(B)/mol |
0 |
0.30 |
0.39 |
0.40 |
0.40 |
下列说法正确的是
A.反应前2min的平均速率v(B)="0.15" mol/(L·min)
B.保持其他条件不变,升高温度,平衡时c(B)="0.22" mol·L-1,则反应的ΔH < 0
C.保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小
D.保持其他条件不变,起始向容器中充入1.2 mol A、0.60 mol B和0.60 mol C,反应达到平衡前的速率:v(正)<v(逆)
反应4NH3+5O2=4NO+6H2O在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率V(x)(表示反应物的消耗速率或生成物的生成速率)
| A.平均速率V(O2)=0.01mol/(L·s) |
| B.平均速率V(NO)=0.008mol/(L·s) |
| C.平均速率V(H2O)=0.002mol/(L·s) |
| D.平均速率V(NH3)=0.002mol/(L·s) |
在2A+B  3C+4D中,表示该反应速率最快的是
3C+4D中,表示该反应速率最快的是
A.υ(A)= 0.5mol·L-1·s-1 B.υ(B)= 0.3 mol·L-1·s-1
C.υ(C)= 0.8mol·L-1·s-1 D.υ(D)=" 1" mol·L-1·s-1
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:X2(g)+ 3Y2(g) 2XY3(g)△H=-92.6 kJ.mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
2XY3(g)△H=-92.6 kJ.mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
| 容器 编号 |
起始时各物质物质的量/mol |
达到平 衡的时间 |
达平衡时体系能量的变化 |
||
| X2 |
Y2 |
XY3 |
|||
| ① |
1 |
3 |
0 |
2分钟 |
放热46.3kJ |
| ② |
0.4 |
1.2 |
1.2 |
/ |
Q(Q>0) |
下列叙述不正确的是
A.容器①中反应从开始到刚达平衡时用XY3表示的反应速率为v(XY3)="1/30" mol·L-1·s-1
B.平衡时,两个容器中XY3的物质的量浓度相等
C.器②中反应达到平衡时吸收的热量为Q
D.容器①体积为0.3L,则达平衡时放出的热量大于46.3kJ
在2A﹢B 2C﹢D反应中,表示该反应速率最快的是
2C﹢D反应中,表示该反应速率最快的是
A.v(A)=0.8mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.6mol·L-1·s-1 D.v(D)=0.5mol·L-1·s-1
一定温度下,在体积为10L的密闭容器中充满NH3,进行如下反应:
2NH3(g) 3H2(g)+N2(g);经5s达到平衡,平衡时NH3和H2的浓度均为bmol/L。下列叙述中不正确的是
3H2(g)+N2(g);经5s达到平衡,平衡时NH3和H2的浓度均为bmol/L。下列叙述中不正确的是
A.NH3在5s内的平均速度为 mol/(L·s) mol/(L·s) |
| B.达到平衡时NH3的分解率为40% |
C.N2的平衡浓度为 mol/L mol/L |
| D.反应开始时与平衡时的压强比为5∶7 |
某反应:2A(g) 3B(g)的各物质的浓度隨时间变化如图所示,则有关反应速率表示正确的是
3B(g)的各物质的浓度隨时间变化如图所示,则有关反应速率表示正确的是

A.v(A)=0.1mol/(L.min)
B.v(B)=0.2mol/(L.min)
C.v(A)=" v(B)" ="0.5" mol/(L.min)
D.v(A)=" v(B)" ="0.3" mol/(L.min)
在恒容密闭容器中,某反应在不同反应时间各物质的量浓度的变化情况如图所示(各物质均为气体)。请回答下列问题:
(1)该反应的化学方程式为 。
(2)反应开始至2分钟时,用C表示反应速率为 mol/(L•min),平衡时A的转化率为 。
(3)其它条件不变,当第3min条件发生以下变化时,能加快化学反应速率的是____。
①加入(正)催化剂 ②充入一定量He
③充入一定量的A ④降低温度
试题篮
()