如图是甲、乙两种固体物质的溶解度曲线.
(1)t2℃时,甲物质的溶解度为 ;
(2)从图中你还能获得哪些信息?(任填一条) ;
(3)分析t1℃时,将10g乙物质放入100g水中,充分溶解后所得的溶液是 (填“饱和”或“不饱和”)溶液.欲使t2℃时乙物质的饱和溶液变为不饱和溶液,可采取的方法 (任填一种方法).
下列数据是氯化钠和氯化铵固体在不同温度时的溶解度
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
10 |
|
| 溶解度/g |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.6 |
77.3 |
(1)医疗上,氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为 。
(2)从海水中提取食盐通常采取晾晒海水的方法而不用降温方法,这是因为随温度升高氯化钠的溶解度变化 (填“大”或“小”)。
(3)20℃时,向100g水中加入25g氯化钠,充分溶解后,溶液中溶质质量分数为 。
(4)现有200g溶质质量分数为10%的氯化钠溶液,若使溶液的溶质质量分数为增大到20%,应该蒸发掉 g水。
(1)宁德毗邻东海,盐资源丰富。
①粗盐提纯主要分为下列三个操作步骤:
请填写操作B的名称 。
②在粗盐提纯的实验中,蒸发滤液时,若等完全蒸干后再停止加热,会导致的后果是 。
A.食盐固体飞溅 B.食盐质量增多 C.食盐溶解
③晒盐后得到的卤水中含有MgCl2、KCl和MgSO4等物质,下图是它们的溶解度曲线示意图:
设t2℃时MgCl2、KCl和MgSO4三种物质的溶解度分别为a、b、c,则a、b、c的大小关系为 。
(2)近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程如下:
①在该“流程图”中,从海水最终得到“NaCl(产品)”的过程属于 (填“物理变化”或“化学变化”)。
②图中反应I、II、III属于化合反应的是 (填序号)。
③反应IV的化学方程式为 。
如图是甲、乙两物质(均不含结晶水)的溶解曲线,据此回答以下问题:
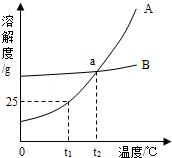
(1)
时,
物质的溶解度为
;
(2)
点的含义是;
(3)溶解度受温度影响小的物质是;
(4)从
、
的混合物中分离
物质,一般采用的方法.
如图是氯化钠与硝酸钾的溶解度曲线,回答下列问题.

(1)配置200g 0.9%的医用生理盐水,需要
的质量为g.
(2)由图可知,
时,硝酸钾的溶解度(填">"、"<"或"=")氯化钠的溶解度;欲提纯混有少量氯化钠的硝酸钾固体,应采用的方法是.
(3)
时,将50g硝酸钾固体完全溶于50g水,形成溶液的质量是.
如图:A,B,C是三种固体物质的溶解度曲线.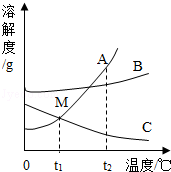
(1)M点表示的意义 .
(2)将t2℃时A,B,C三种物质的饱和溶液均降温到t1℃时,溶质质量分数最小的是 .
(3)当A物质中混有少量B物质时,提纯A物质的方法是 .
废电池随意丢弃不仅造成环境污染,还会造成资源浪费.废电池内的黑色物质含有碳、二氧化锰、氯化铵等物质.氯化铵浓溶液可用于除某些金属表面的氧化物.某研究小组要回收和利用废电池内的氯化铵,进行如图1所示实验:

(1)操作②的名称是.
(2)小组同学欲配制30℃的氯化铵饱和溶液来除金属表面的氧化物.查氯化铵的溶解度图(如图2所示)可知:30℃时,100克水中最多能溶解克氯化铵.
(3)用氯化铵(
)浓溶液去除某金属表面氧化物(氧化物化学式用
表示),其反应原理为:
↑,则物质
的化学式为。
如图所示是
三种物质的溶解度曲线,据此图回答:

(1)
℃时,
三种物质的溶解度由大到小的顺序是;
(2)
℃时,将
放入
水中,充分搅拌后,所得溶溶液的溶质质量分数是;
(3)
℃时,将等质量
两种物质的饱和溶液降温到
℃时,析出晶体质量较大的是;
(4)
℃时,将
放入
水中,充分搅拌后得到
的饱和溶液,在不改变溶剂量的前提下,将其变为不饱和溶液的方法是.
根据固体物质
在水中的溶解度曲线图,回答下列问题:

(1)
点所表示的溶液为
在
℃的(选填"饱和"或"不饱和")溶液.
(2)将
点对应的溶液从
℃升温到
℃(忽略水的蒸发),在此过程中
的质量分数(选填"增大"、"减小"或"不变");
(3)将
点对应的
溶液恒温蒸发
水,可析出
的质量为g,剩下的溶液中
的质量分数为.
如图为甲、乙两种固体物质的溶解度曲线(水的密度约为
).

(1)两种物质中,溶解度受温度影响更大的是(填"甲"或"乙").(2)20
时,乙的溶解度为.
(3)下列实验中:10
水

 为饱和溶液的是(填"
"或"
"或"
");若三中溶液中溶质的质量分数分别为
、
、
,则它们的大小关系是(用"<"或">"或"="表示出来)
为饱和溶液的是(填"
"或"
"或"
");若三中溶液中溶质的质量分数分别为
、
、
,则它们的大小关系是(用"<"或">"或"="表示出来)
水是一种重要的自然资源,与人类的生产、生活密切相关.
(1)降雨是自然界中水循环的一个环节,请用分子运动的观点解释这一变化过程.
(2)
的降水称为酸雨,要检验某次降水是否是酸雨,正确的操作为.
(3)水是常用的溶剂。向20mL水中溶解一定量
固体的操作如下,请根据实验现象和溶解度曲线回答下列问题(水的密度以1g/mL计):
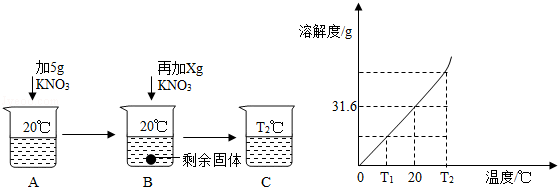
A、B、C中溶液一定是饱和溶液的是,一定是不饱和溶液的是;当
g时,
中恰好没有固体剩余.
按要求完成下列小题:
如图所示,
两种固体物质的溶解度曲线:

①
两种物质的溶解度都随温度的升高而,其中溶解度受温度影响较大的是;
②已知t℃时,
物质的溶解度为
.则t℃时,
物质饱和溶液中溶质质量分数可以表示为%;
③气体的溶解度常用体积来表示,如0℃时,氮气的溶解度为0.023,其含义是.
(2)现有两瓶失去标签的溶液,溶质分别可能是硝酸钠、硝酸铜、硝酸、硫酸钠、硫酸、碳酸钾中的一种,检验步骤如下:
Ⅰ.分别取少量混合,无明显现象,溶液无色透明,经测定混合溶液显酸性.由此可推断这两瓶溶液中的溶质一定不是;(填化学式,多填、少填、错填均不得分,下同)
Ⅱ.向上述混合溶液中加入
溶液,产生白色沉淀.则这两瓶溶液中的溶质至少是中的一种;
(3)将
三种物质各
混合,一定条件下充分反应后,测得混合物中有
和一定质量的
完全反应.若
的相对分子质量之比为8:16:22:9,则该反应的化学方程式可表示为.
下表是
的溶解度数据,请分析回答:
| 温度/℃ |
10 |
20 |
30 |
40 |
| 溶解度/g |
31.0 |
34.0 |
37.0 |
40.0 |
(1)
时,100g水中最多能溶解g固体
.
(2)
时,将25
固体
与50
水混合,充分搅拌,所得的溶液是溶液(填"饱和"或"不饱和").
如图是硝酸钾和氯化钠的溶解曲线图,根据图象回答:

(1)t°C,
的溶解度(填"〉""等于"或"〈")
的溶解度.
(2)
溶液中含少量的
,将
从溶液中析出,常用(填"降温"或"蒸发")结晶.
(3)向某温度下的
饱和溶液中加入
晶体,则
(填"能"或"不能")溶解.
(4)读图,你能获取的一条信息是.
甲、乙、丙三种物质的溶解度曲线如图所示,据图回答下列问题:

(1)
时,甲物质的溶解度是.
(2)
时,甲、乙、丙三种物质的溶解度由大到小的顺序是.
(3)要使
时接近饱和的丙溶液变成饱和溶液,可采用的一种方法是.
(4)向100g
时的水中,加入31g甲固体充分搅拌,发现甲全部溶解,一段时间后又有部分甲析出.你认为甲开始能"全部溶解"的原因可能是.
试题篮
()