根据表中信息判断,下列选项不正确的是 ( )。
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4…… |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4-…… |
Cl2、Mn2+…… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱的顺序为MnO4->Cl2>Fe3+>Br2
新型纳米材料MFe2O,(3<x <4)中M表示十2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,转化过程为:
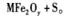 下列判断正确的是
下列判断正确的是
| A.MFe2Ox是还原剂 | B.SO2被氧化 |
| C.x>y | D.氧化性:MFe2Oy>SO2 |
O3具有强氧化性,将O3通入KI溶液中发生反应:O3+I-+H+―→I2+O2+H2O(未配平),下列说法正确的是 ( )。
| A.配平后的离子方程式为2O3+2I-+4H+=I2+2O2+2H2O |
| B.每生成1 mol I2转移电子2 mol |
| C.O2是还原产物之一 |
| D.该反应能说明O2的氧化性大于I2的 |
常温下,在溶液中可发生以下反应:
①16H++10Z-+2XO4-===2X2++5Z2+8H2O;
②2M2++R2===2M3++2R-;
③2R-+Z2===R2+2Z-。
由此判断下列说法错误的是
| A.常温下可发生反应2M2++Z2===2M3++2Z- |
| B.还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C.Z元素在反应①中被氧化,在③中被还原 |
| D.氧化性强弱顺序为:XO4-<Z2<R2<M3+ |
铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:(1)Tl3++2Ag=Tl++2Ag+,(2)Ag++Fe2+=Ag+Fe3+,(3)Fe+2Fe3+=3Fe2+,下列离子氧化性比较顺序正确的是 ( )。
| A.Tl3+>Fe3+>Ag+ | B.Fe3+>Ag+>Tl3+ |
| C.Tl+>Ag+>Fe2+ | D.Tl3+>Ag+>Fe3+ |
根据下列反应判断有关物质还原性由强到弱的顺序正确的是
(1)H2SO3 + I2 + H2O =" 2HI" + H2SO4
(2)2FeCl3 + 2HI = 2FeCl2 + 2HCl + I2
(3)3FeCl2 + 4HNO3 = 2FeCl3 + NO↑+ 2H2O + Fe(NO3)3
| A.H2SO3>I->Fe2+>NO |
| B.I->H2SO3>Fe2+>NO |
| C.Fe2+>I->H2SO3>NO |
| D.NO>Fe2+>H2SO3>I- |
已知常温下,在溶液中可发生如下反应: 
Ce4+ + Fe2+ = Fe3+ + Ce3+, Sn2+ + 2Fe3+ = 2Fe2+ + Sn4+
由此推断Fe2+ 、Ce3+、 Sn2+的还原性由强到弱的顺序是 ( )
| A.Sn2+、Fe2+ 、Ce3+ | B.Fe2+ 、Ce3+、 Sn2+ |
| C.Fe2+ 、Sn2+、Ce3+ | D.Ce3+、Fe2+ 、Sn2+ |
由相同条件下的三个反应:2A-+B2=2B-+A2;2C-+A2=2A-+C2;2B-+D2=2D-+B2可以判断正确的是( )
| A.氧化性:A2>B2>C2>D2 | B.还原性:A->B->C->D- |
| C.2A-+D2=2D-+A2反应可以进行 | D.2C-+B2=2B-+C2反应不能进行 |
①A+B2+ =A2++B , ②D +2H2O=D(OH)2 + H2↑,③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-="E" ,B—2e-=B2+
A.E2+>B2+>A2+>D2+ B.D2+>E2+>A2+>B2+
C.D2+>B2+>A2+>E2+ D.A2+>B2+>D2+>E2+
已知:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O,MnO2+4HCl MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
MnCl2+Cl2↑+2H2O。其中KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol·L-1)反应,MnO2需和浓盐酸(>8 mol·L-1)反应。根据以上信息,下列结论中不正确的是 ( )。
| A.上述反应均属于氧化还原反应 |
| B.生成1 mol Cl2时,三个反应中转移的电子数相等 |
| C.盐酸浓度越大,Cl-的还原性越强 |
| D.氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 |
常温下溶液中可发生如下反应:①16H++10Z-+2XO4-=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-,由此判断下列说法错误的是( )
| A.反应Z2+2A2+=2A3++2Z-可以进行 |
| B.Z元素在①③反应中均被还原 |
| C.氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ |
| D.还原性由强到弱顺序是A2+、B-、Z-、X2+ |
臭氧具有强氧化性,可使湿润的碘化钾淀粉试纸变蓝,有关反应如下:
O3 + 2KI + H2O =" 2KOH" + I2 + O2,对于此反应下列说法正确的是
| A.反应中O3是氧化剂,H2O和KI是还原剂 |
| B.在反应中,每消耗1molO3转移2mol电子 |
| C.氧化产物I2和还原产物O2的物质的量之比为1∶1 |
| D.由此反应可知,氧化性强弱顺序为O3>I2>O2 |
已知:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3。下列粒子的氧化性从强到弱的顺序正确的是
| A.Cl2>Fe3+>I2 | B.I2>Cl2>Fe3+ |
| C.Fe3+>Cl2>I2 | D.Cl2>I2>Fe3+ |
碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种微粒之间有如图所示关系,根据图示转化关系推测下列说法不正确的是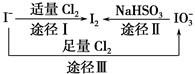
| A.可用KI淀粉试纸和食醋检验加碘盐中是否含有碘 |
| B.足量Cl2能使湿润的KI淀粉试纸变白的原因可能是: 5Cl2+I2+6H2O===2HIO3+10HCl |
| C.由图可知氧化性的强弱顺序为Cl2>I2>IO3- |
| D.途径Ⅱ中若生成1 mol I2,反应中转移的电子数为10NA |
根据下列反应,可以判断有关物质的氧化性由强到弱的顺序正确的是( )。
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S↓+2HI
| A.H2S>I2>Fe3+>Cl2 | B.Cl2>Fe3+>I2>S |
| C.Fe3+>Cl2>H2S>I2 | D.Cl2>I2>Fe3+>H2S |
试题篮
()